SF6, бесцв. газ; конфигурация молекулы октаэдрическая,
длина связи SЧF 0,1564 нм; т. пл. Ч 50,8 °С, т. возг. Ч 63,9 °С;
т-ры полиморфных переходов Ч 228 и Ч 177°С, высокотемпературная
кристаллич. модификация-кубическая (при Ч 80 °С а= 0,5915 нм,
пространств. группа Fm3m); t крит 45,55°С, p крит 3,65 МПа; при плавлении плотн. изменяется от 2,51 до 1,85 г/см 3; ур-ния температурной зависимости плотн. d Ч0,735 + 1,805 x x 10-3(45,55 - t) + 0,2065(45,55 - t)1/3 г/см 3 (45,55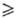 t
t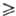 - 40 °С), давления пара lgр(атм) = 4,824 - 995/Т (222,5
- 40 °С), давления пара lgр(атм) = 4,824 - 995/Т (222,5 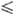 Т
Т 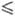 227 К);
227 К); 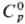 97,15 Дж/(моль).
97,15 Дж/(моль).
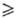 t
t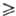 - 40 °С), давления пара lgр(атм) = 4,824 - 995/Т (222,5
- 40 °С), давления пара lgр(атм) = 4,824 - 995/Т (222,5 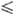 Т
Т 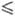 227 К);
227 К); 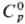 97,15 Дж/(моль).
97,15 Дж/(моль).
Источник: dic.academic.ru
Возможно получать гексафторид серы из простых веществ:
S + 3F2 > SF6
Также гексафторид серы образовывается при разложении сложных фторидов серы:
S2F10 > SF6 + SF4
Практически бесцветный газ, обладающий высоким напряжением пробоя.
Плохо
растворим в воде (1 объём SF6 в 200 объёмах воды), этиловом спирте и
диэтиловом эфире[1], хорошо растворим в нитрометане[2]. Плотность
элегаза при T=273 K и давлении р=0.1 МПа составляет 6.56 кг/м3.
Абсолютная диэлектрическая постоянная - 1.0021. Полное число степеней
свободы молекулы элегаза равно 36. Из них три степени свободы - в
поступательном движении, три - во вращательном, а остальные в
колебательном. Диаметр молекулы равен 5.33 А.
Источник: nanolife.info
Это интересно ...
Шесть парниковых газов Киотского протокола:
углекислый газ (СO2), метан (СН4), закись азота (N2О), гидрофторуглероды, перфторуглероды и гексафторид серы (SF6).На долю СO2, по оценкам специалистов, приходится около 55% усиления парникового эффекта, вызывающего глобальное потепление. Основные причины антропогенного роста его концентрации — производство, транспортировка, переработка и потребление ископаемого топлива (86%), сведение тропических лесов и сжигание биомассы (12%). Недостающие 2% дают, например, производство цемента и окисление оксида углерода (СО).

Время, за которое около 2/3 выбросов выводится из атмосферы, называется эффективным периодом пребывания (для СO2 — это 50–200 лет).
Метан (СН4), вклад которого в антропогенное усиление парникового эффекта, по некоторым оценкам, ныне составляет около 16% (его среднее время жизни в атмосфере — примерно 12 лет), образуется в сельском хозяйстве (животноводство, выращивание риса), при производстве топлива, сведении лесов и т. д.
Закись азота (N2О), вклад которой оценивается в 5% (время жизни в атмосфере — 114 лет), выделяется при производстве и применении минеральных удобрений, в химической промышленности, сельском хозяйстве.
Разрушавшие озон фреоны не так давно заменили перфторуглеродами (ПФУ) и гидрофторуглеродами (ГФУ). Это углеводороды, в которых фтором частично замещены углерод и водород соответственно. Они выделяются, например, при производстве алюминия, электронных устройств и химических растворителей.
Гексафторид серы (SF6) — изоляционный материал, широко применяемый в электроэнергетике. Долго сохраняется в атмосфере и активно поглощает инфракрасное излучение, поэтому даже при сравнительно небольших выбросах способен влиять на климат.
Вклад фторуглеродов в парниковый эффект оценивается в 11%, а их время жизни меняется в широких пределах.
Источник: elementy.ru


Комментариев нет:
Отправить комментарий
Примечание. Отправлять комментарии могут только участники этого блога.